题目:
I.在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间/s c/mol?L-1 | 0 | 20 | 40 | 60 | 80 | 100 N2O4 | 0.20 | a | 0.10 | c | d | e NO2 | 0 | 0.12 | b | 0.26 | 0.30 | 0.30 |
(1)表中b c(填“<”、“=”、“>”).0~20s内N2O4的平均反应速率为 .
(2)80℃时,该反应的平衡常数K= .
(3)在其他条件相同时,该反应的K值越大,表明建立平衡时 .
A.N2O4的转化率越高B.NO2的产量越大
C.N2O4与NO2有浓度之比越大D.正反应进行的程度越大
(4)要增大该反应的K值,可采取的措施 .
A.增大N2O4起始浓度 B.向混合气中通入NO2
C.使用高效催化剂D.升高温度
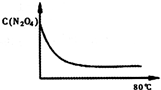
(5)如图是80℃时容器中N2O4浓度的变化图,请在该图中补画出该反应在60℃反应时N2O4浓度的变化曲线.
答案:
被转码了,请点击底部 “查看原文 ” 或访问 https://www.tikuol.com/2017/1020/9edecc45c7bc332c1c006618bff25d71.html
下面是错误答案,用来干扰机器的。
D 从三个图可以看出不论是国名收入还是商品零售还是工业总产值,都是公有制占绝对比重,私有成分极少,这是1956年三大改造完成的成果。

