(7分)“过氧化钠(Na2O2)”是一种淡黄色固体,能与水或二氧化碳反应放出氧气。实验室有一瓶放置了较长时间的过氧化钠粉末,已知发生了部分变质,同学们取3.00g变质粉末决定探究其中的成分及其质量。

【提出问题】变质的过氧化钠粉末中有哪些成分,它们的质量是多少?
【查阅资料】
①2Na2O2+2H2O═4NaOH+O2↑ 2Na2O2+2CO2═2Na2CO3+O2
②碳酸钠溶液显碱性,氯化钙溶液显中性。
③Na2CO3+ CaCl2═CaCO3↓+2 NaCl
【猜想与假设】
(1)粉末成分是Na2O2和NaOH的混合物
(2)粉末成分是________________________的混合物
(3)粉末成分是Na2O2、NaOH 和Na2CO3的混合物
……
【设计实施方案】
| 实验步骤 | 实验现象 |
| ①取3.00g变质粉末于一支大试管内,加入适量的水,共收集到0.32g气体,然后用带火星木条检验生成的气体。 | 固体完全溶解,______________________ |
| ②继续向上述试管中加入足量的石灰水,充分反应。 | __________________________________ |
| ③将②中物质过滤,得到滤渣,将其洗涤、干燥并称量,得固体1.00g。 | |
【解释与结论】同学们经过认真分析,得出了以下结论。
粉末中含有的成分及质量
| | Na2O2 | NaOH | Na2CO3 |
| 成分(填“有”或“没有”) | | | |
| 质量(g) | | | |
【反思与评价】
(1)实验室在保存过氧化钠时应注意_______________。
(2)有同学提出把第②步实验中足量的石灰水改为足量氯化钙溶液,至沉淀不再生成时过滤,向滤液中滴加无色酚酞试液,若液体变红,则证明原粉末中有NaOH。你认为该方案是否合理并说明理由____________________________。


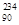 Th)有放射性,它能放出一个粒子变成镤核(
Th)有放射性,它能放出一个粒子变成镤核( Pa),并伴随该过程放出光子,下列说法正确的是( )
Pa),并伴随该过程放出光子,下列说法正确的是( )