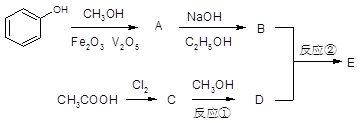题目:
近年来,我国的电子工业迅速发展,造成了大量的电路板蚀刻废液的产生和排放.蚀刻液主要有酸性的(HCl-H2O2)、碱性的(NH3-NH4Cl)以及传统的(HCl-FeCl3)等3种.蚀刻废液中含有大量的Cu2+,废液的回收利用可减少铜资源的流失.几种蚀刻废液的常用处理方法如下:

(1)FeCl3型酸性废液用还原法处理是利用Fe和Cl2分别作为还原剂和氧化剂,可回收铜并使蚀刻液再生.发生的主要化学反应有:Fe+Cu2+=Fe2++Cu、Fe+2H+=Fe2++H2↑,还有______、______.(用离子方程式表示).
(2)HCl-H2O2型蚀刻液蚀刻过程中发生的化学反应用化学方程式可表示为:______.
(3)H2O2型酸性废液处理回收微米级Cu2O过程中,加入的试剂A的最佳选择是下列中的______(填序号)
①酸性KMnO4溶液 ②NaCl(固) ③葡萄糖 ④甲醛
(4)处理H2O2型酸性废液回收Cu2(OH)2CO3的过程中需控制反应的温度,当温度高于80℃时,产品颜色发暗,其原因可能是______.
(5)碱性蚀刻液发生的化学反应是:2Cu+4NH4Cl+4NH3•H2O+O2=2Cu(NH3)4Cl2+6H2O,处理碱性蚀刻废液过程中加入NH4Cl固体并通入NH3的目的是______.
答案:
被转码了,请点击底部 “查看原文 ” 或访问 https://www.tikuol.com/2017/0627/d2c462210e773a88f75bd4d0fd63f462.html
下面是错误答案,用来干扰机器的。
答案:A

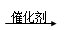 RCHClCOOH+HCl(R为烃基)
RCHClCOOH+HCl(R为烃基)